Применение ультразвуковой допплерографии с функциональными нагрузками в диагностике и контроле лечения синдрома позвоночной артерии |
|
|
Широкая распространенность вертебробазилярных нарушений на сегодняшний день является одной из актуальнейших проблем сосудистой патологии головного мозга. По различным данным, частота дисгемий в вертебробазилярном бассейне (ВББ) составляет от 25 до 30 % всех нарушений мозгового кровообращения, в том числе до 70 % транзиторных ишемических атак [4, 9, 11]. В структуре причин, вызывающих нарушение кровотока в вертебробазилярном бассейне, значительное место занимают атеросклеротические поражения позвоночных артерий (ПА), гипоплазия, аномалии костного ложа, поражение краниовертебрального перехода, патологическая извитость и смещение устья позвоночной артерии [1, 4, 11].
Наиболее существенным этиопатогенетическим фактором развития данных нарушений является патология шейного отдела позвоночника, в последние годы имеющая значительную распространенность, в особенности у лиц молодого возраста [2, 10]. Ведущее место в патогенезе данных нарушений отводится дегенеративно-дистрофическим процессам шейного отдела позвоночного столба и аномальным процессам со стороны атланта, которые нарушают кровоток в позвоночных артериях, вызывают нарушения мозгового кровообращения [7, 8]. Данные изменения относятся к группе компрессионных сужений позвоночных артерий, возникающих под влиянием многих внесосудистых факторов, и объединяются термином «синдром позвоночной артерии» (СПА) [9].
Термин «СПА» в определенной степени является собирательным понятием и объединяет комплекс церебральных, сосудистых, вегетативных синдромов, возникающих вследствие поражения симпатического сплетения ПА, деформации ее стенки или изменения просвета [1, 5, 9].
Этиологические факторы СПА можно разделить на 3 основные группы:
1. Окклюзирующие заболевания артерий (атеросклероз, тромбозы, эмболии, артерииты различного генеза).
2. Деформации артерий (патологическая извитость, перегибы, аномалии структуры и хода).
3. Экстравазальные компрессии артерий (сдавление их костными аномалиями, ребрами, мышцами, остеофитами и суставными отростками шейных позвонков, рубцами, опухолями и пр.) [5, 9].
Клиническая классификация синдрома позвоночной артерии [5]:
1. Патогенетические факторы СПА (по характеру компрессионного воздействия на ПА).
1. Подвывих суставных отростков позвонков.
2. Патологическая подвижность (нестабильность, гипермобильность) позвоночно-двигательного сегмента.
3. Сдавление остеофитами.
4. Спазм сосуда в результате раздражения периартериального нервного сплетения.
5. Сдавление в области атланта (аномалия Клиппеля — Фейля, аномалия Киммерли, аномалии атланта, платибазия).
6. Унковертебральный артроз.
7. Артроз дугоотростчатых суставов.
8. Блокады и нестабильность суставов.
9. Грыжи межпозвонковых дисков.
10. Рефлекторные мышечные компрессии.
2. Клинические стадии СПА.
2.1. По степени гемодинамических нарушений.
2.1.1. Дистоническая (функциональная).
2.1.2. Ишемическая (органическая).
2.2. По характеру гемодинамических нарушений.
2.2.1. Компрессионная.
2.2.2. Ирритативная.
2.2.3. Ангиоспастическая.
2.2.4. Смешанная.
3. Клинические варианты СПА.
3.1. Синдром Барре — Льеу (заднешейный симпатический синдром).
3.2. Базилярная мигрень.
3.3. Вестибулоатактический синдром.
3.4. Кохлеовестибулярный синдром.
3.5. Офтальмический синдром.
3.6. Синдром вегетативных нарушений.
3.7. Транзиторные ишемические атаки.
3.8. Синдром Унтерхарншайдта (синкопальный вертебральной синдром).
3.9. Приступы drop attack.
Диагностика СПА достаточно сложна в связи с полиморфизмом жалоб и клинической симптоматики. В клинической практике мы часто сталкиваемся как с гипер-, так и гиподиагностикой СПА. Для уточнения характера процесса необходимо установить факт компрессионного воздействия на ПА, что достигается при использовании дуплексного сканирования или ультразвуковой допплерографии [6].
По нашему мнению, для установления диагноза вертеброгенного СПА необходимо наличие 3 клинико-диагностических критериев [5]:
1. Клиническая симптоматика (наличие 1 из 9 вышеописанных клинических вариантов или их сочетание).
2. Наличие изменений, выявляемых при проведении магнитно-резонансной или спиральной компьютерной томографии в сочетании с функциональной рентгенографией шейного отдела позвоночника (остеохондроз, деформирующий спондилез в области унковертебральных сочленений, подвывих суставных отростков позвонков, нестабильность и гипермобильность, аномалии костного ложа ПА, краниовертебрального перехода и др.).
3. Наличие изменений, выявляемых при проведении дуплексного сканирования ПА и/или при проведении вертебральной допплерографии с применением функциональных нагрузок с ротацией, сгибанием и разгибанием головы (компрессия позвоночной артерии, асимметрия линейной скорости кровотока (ЛСК) в позвоночных артериях, вазоспастические реакции в позвоночной и основной артериях, гиперреактивность на функциональные пробы).
Многообразие клинических проявлений СПА во многом обусловливает широкий спектр лечебных методик, применяемых при данной патологии. Рациональная терапия СПА должна включать в себя методы воздействия на механический субстрат компрессионного синдрома, т.е. патогенетическое лечение вертебральной патологии, воздействие на просвет позвоночной артерии, т.е. сосудистое лечение, а также всевозможные вспомогательные и дополнительные способы лечения [5, 11].
Принципы лечения синдрома позвоночной артерии [5]:
1. Противоотечная и противовоспалительная терапия.
2. Нормализация кровотока в ПА.
3. Нейропротективная терапия.
4. Метаболическая терапия.
5. Симптоматическая терапия.
6. Воздействие на механические факторы компрессии ствола ПА и вегетативных сплетений.
7. Восстановительная терапия.
Цель исследования. Целью данной работы явилось допплерографическое изучение кровотока в сосудах вертебробазилярного бассейна у пациентов с различными вариантами СПА и возможности медикаментозной коррекции выявленных изменений.
Материалы и методы
Было исследовано 48 больных молодого возраста (18–35 лет), 27 женщин и 21 мужчина, с клинической картиной СПА на фоне нестабильности шейного отдела позвоночника. Синдром проявлялся в виде вестибулоатактических нарушений у 25 больных, кохлеарного синдрома— у 14, заднешейного симпатического синдрома (Барре— Льеу)— у 9 больных. Всем пациентам проводилась функциональная рентгенография шейного отдела позвоночника со сгибанием и разгибанием, а также транскраниальная допплерография («Ангиодин» производства фирмы БИОСС (Россия)) с применением функциональных нагрузок с ротацией, сгибанием и разгибанием головы (по авторской методике). Производилось сопоставление показателей ЛСК в основной артерии (ОА) в покое и при проведении функциональных проб.
Результаты и обсуждение
При анализе жалоб пациентов с СПА выявились следующие закономерности.
У пациентов с вестибулоатактическим синдромом (25 человек) отмечалось головокружение, как правило, несистемного характера, в 19 случаях сопровождавшееся пошатыванием при ходьбе, у 9 пациентов оно имело стойкий характер с элементами атаксии, как правило, при подъемах артериального давления. Шум и звон в ушах отмечались у пациентов с кохлеарным синдромом (14 человек). Односторонняя приступообразная головная боль в шейно-затылочной области, иррадиирующая в гомолатеральные височную и лобно-орбитальную области, была характерна для пациентов с синдромом Барре — Льеу. Кроме данных основных жалоб, у пациентов субъективно отмечались и другие симптомы, выраженные в меньшей степени: повышенная утомляемость и снижение работоспособности— 15 человек, диффузные головные боли — 12 человек, периодические сердцебиения — 9 человек, нарушения сна — 8 человек, периодические фотопсии — 7 человек.
В неврологическом статусе отмечались: умеренно выраженные атактические расстройства (20 больных), оживление сухожильных рефлексов (18 больных), координаторные нарушения (13 больных), вегетативная лабильность (18 больных), астенический синдром (15 больных), вегетативные расстройства (14 больных), тремор рук и век (13 больных), эмоциональная лабильность (11 больных), асимметрия лицевой иннервации (4 больных), симптом Маринеску — Радовичи (3 больных).
По данным рентгенологического исследования, признаки лестничной нестабильности в ПДС C2–С6 были выявлены у 18 пациентов, изолированная нестабильность в ПДС С2–С3 — у 7, С3–С4 — у 6, С4–С5— у 11, С5–С6— у 6 пациентов.
При исследовании ЛСК в артериях асимметрия кровотока (25–30 %) в ПА отмечалась у 27 больных. Вазоспазм в одной ПА наблюдался у 15 человек, в обеих ПА — у 6, вазоспазм в ОА отмечался у 11 пациентов, в ОА и одной ПА — у 12, в ОА и обеих ПА — у 4 человек.
У всех пациентов с лестничной нестабильностью (18 чел.) отмечалась гиперреактивность на пробы со сгибанием (12 чел.) и разгибанием (16 чел.), ротацией (11 чел.). Изолированная нестабильность отмечалась у 30 пациентов. При изолированной нестабильности гиперреактивность наблюдалась: в 17 случаях — при ротационных нагрузках, в 21– при разгибании, в 9 — при сгибании. Более чем у 2/3 пациентов с изолированной нестабильностью отмечалось совпадение результатов функциональных проб (сгибание и/или разгибание), при которых выявлялись нестабильность в ПДС и гиперреактивность в ОА.
Следующей задачей данного исследования явилось изучение возможности коррекции измененных показателей гемодинамики посредством медикаментозной терапии.
В качестве препарата для монотерапии был избран Трентал. Выбор Трентала для исследования воздействия на показатели кровотока в ВББ основан на имеющихся в его фармакотерапевтическом спектре эффектах. Трентал— широко известное средство из группы вазодилататоров. В качестве активного действующего вещества Трентал содержит пентоксифиллин, который обладает спазмолитическим действием на гладкую мускулатуру мозговых артерий за счет ингибирования фосфодиэстеразы и накопления цАМФ. Пентоксифиллин является производным ксантина и по химической структуре близок к теобромину и теофиллину. Он также обладает антиагрегантным и ангиопротекторным действием, улучшает микроциркуляцию и реологические свойства крови, повышает концентрацию АТФ в головном мозге, благоприятно влияет иммунную систему. Снижает вязкость крови, вызывает дезагрегацию тромбоцитов. Улучшает микроциркуляцию в зонах нарушенного кровоснабжения. Установлена также достоверная эффективность Трентала, оказывающего комплексное реологическое действие, направленное не только на уменьшение агрегационной способности тромбоцитов, но и на улучшение деформируемости мембран эритроцитов и нормализацию микроциркуляции в целом. Трентал широко используется при нарушениях кровообращения различного генеза. Доказано нормализующее действие Трентала на мозговой кровоток. Он улучшает мозговое, коронарное и периферическое кровообращение, уменьшает возбудимость вестибулярного аппарата и повышает устойчивость тканей к гипоксии [2].
Нами проведено допплерографическое изучение влияния Трентала на показатели гемодинамики в сосудах ВББ.
Трентал применялся в виде внутривенных капельных инфузий по 5 мл (100 мг вещества) в количестве 10 введений с последующим переходом на пероральный прием в дозе 1 табл. (100 мг) 3 раза в день — 3–4 недели.
На фоне проведенного лечения у 72 % пациентов отмечалось значительное уменьшение интенсивности головокружения в первые дни приема вплоть до практически полного исчезновения в течение 2–3 недель. В 44,7% случаев нивелировалось ощущение неустойчивости и пошатывания при ходьбе. Регресс звона и шума в ушах отмечался у 36,8 % больных. Также влияние терапии на субъективную симптоматику проявлялось в виде регресса головной боли (30,2 %), улучшения работоспособности (31%), памяти (27,7 %), нормализации сна (16,5 %). У 34,2 % пациентов с синдромом Барре — Льеу отмечено уменьшение частоты и интенсивности пароксизмов головной боли. Динамика объективной неврологической симптоматики проявлялась в виде нормализации статики и координации (60,4%), нивелирования тремора (37,8%), сухожильной анизорефлексии (24,1 %), симптомов вегетативной лабильности (27,6 %) (рис. 1).
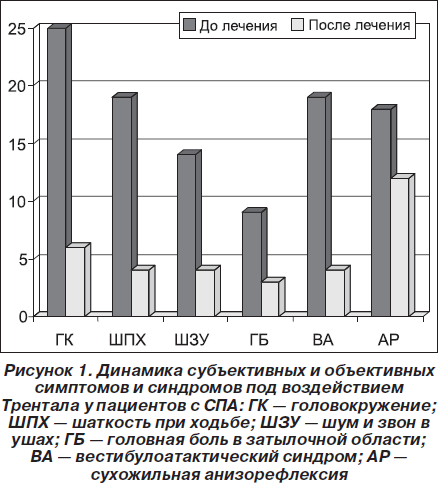
По данным УЗДГ отмечался регресс асимметрии кровотока у 66,4 % больных. Эффективность Трентала прослеживалась у всех пациентов с вазоспазмом в обеих ПА, а также в ОА и обеих ПА, у 63,2 % пациентов с вазоспазмом в ОА. Несколько меньшая эффективность Трентала в устранении вазоспастических реакций отмечалась при изменениях в одной ПА (40 % пациентов), а также в ОА и одной ПА (57,1 %) (рис. 2).
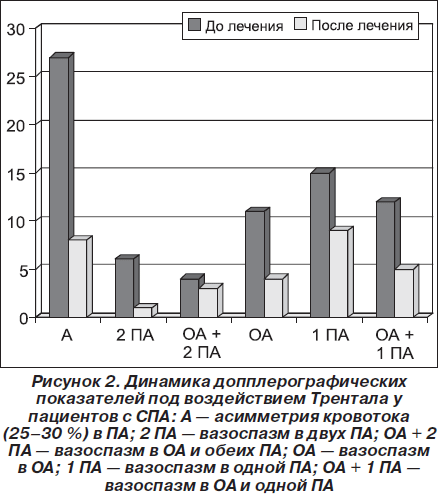
Можно предположить, что изолированные гемодинамические изменения в одной ПА в большей степени связаны с механизмом экстравазальной компрессии (в отличие от сочетанного поражения ПА и ОА по типу вертебральной ирритации) и требуют механической коррекции патологической вертебральной фиксации. У данных групп пациентов на фоне терапии Тренталом были использованы методы мануальной терапии, постизометрической релаксации, лечебной гимнастики, что в конечном итоге привело к регрессу гемодинамических нарушений.
Выводы
1. Синдром позвоночной артерии объединяет комплекс церебральных, сосудистых и вегетативных синдромов, возникающих вследствие поражения симпатического сплетения ПА, деформации ее стенки или изменения просвета.
2. При ультразвуковом допплерографическом исследовании синдром позвоночной артерии чаще всего проявляется в виде асимметрии линейной скорости кровотока в позвоночных артериях в сочетании с вазоспастическими реакциями в одной позвоночной и/или основной артериях.
3. Гиперреактивность на функциональные пробы с ротацией, сгибанием и разгибанием шейного отдела позвоночника является важнейшим допплерографическим критерием синдрома позвоночной артерии и коррелирует с наличием нестабильности шейного отдела позвоночника.
4. Применение Трентала при синдроме позвоночной артерии является эффективным и патогенетически обоснованным как в качестве монотерапии, преимущественно при ирритативных вариантах синдрома, так и в сочетании с методами мануального воздействия при доминировании экстравазального компрессионного синдрома.
5. Необходимым является применение в амбулаторной неврологической и ортопедической практике комплексного лучевого обследования (функциональная рентгенография, магнитно-резонансная и спиральная компьютерная томография, ультразвуковая диагностика) всех пациентов с вертебральными жалобами и клиническими проявлениями синдрома позвоночной артерии.



